Dr M.Gourmelon, Dr C.Bour
14 mars 2020
Après la parution de notre lettre commune co-rédigée avec 4 autres collectifs européens, lettre publiée dans le journal médical français JIM et reprise dans le BMJ, (en français). Le Dr DELALOGE coordonatrice française de l'étude MyPEBS, y a répondu dans une dépêche Apm du 02/03/2020.
Nous répondons en retour à ses arguments en nous basant aussi sur ses propos repris dans l'article du BMJ du 03/03/2020.
EFFICACITE DU DEPISTAGE
Dans l'article du BMJ Mme Delaloge s'appuie sur le fait que le dépistage actuel est le standard requis dans plusieurs pays et, comme il est précisé dans la dépêche, il n'est nullement question de le remettre en cause mais plutôt de tenter son amélioration.
"While there were clear benefits from breast cancer screening in terms of reduced breast cancer specific mortality", she said, “we need to improve on what currently exists, but we cannot have an arm in which screening would disappear. That would not be ethical at all.”
"Bien que le dépistage du cancer du sein présente des avantages évidents pour ce qui est de la réduction de la mortalité spécifique au cancer du sein", elle a déclaré : « nous devons améliorer ce qui existe actuellement, mais nous ne pouvons pas avoir un bras dans lequel le dépistage disparaîtrait. Ce ne serait pas du tout éthique.»
Cette affirmation selon laquelle le dépistage du cancer du sein présente des avantages évidents est contestée par de nombreuses études scientifiques indépendantes, donc affirmer que le dépistage présente des avantages évidents est une position uniquement partagée par les promoteurs de ce même dépistage. Ce n'en fait donc pas une réalité "évidente".
Nous reviendrons sous peu sur l'argument de l'éthique.
Le dépistage standard sert actuellement de socle.
Or le standard (ce qui se fait quotidiennement) n'est pas forcément ce qui devrait être fait.
Même si le dépistage actuel est validé par les autorités sanitaires et les sociétés savantes, on ne peut ignorer de très nombreuses études qui infirment son utilité en terme de réduction de la mortalité et des cancers graves.
Cette contestation scientifique est internationale et loin d’être minoritaire.
D’ailleurs même en France a eu lieu en 2015/2016 une concertation citoyenne sur le dépistage du cancer du sein, dont les deux scénarios demandaient son arrêt.(page 133 du rapport)
Cette contestation, de plus en plus pressante, aboutit même, dans certains pays (Australie, Québec) à des plans nationaux de réduction de la surmédicalisation tellement le fardeau aussi bien en santé humaine que sur le plan économique apparaît lourd.
Le bénéfice en matière de réduction de mortalité invoqué par le Dr DELALOGE repose sur une publication qu'elle a cité à plusieurs reprises déjà, publiée dans le European Journal of Cancer :
ZielonkeN,GiniA,JansenEEL,et al.Evidenceforreducing cancer-specificmortalitydueto screeningforbreastcancer in Europe: A systematicreview.Eur JCancer.2020;127:191–206.doi:10.1016/j.ejca.2019.12.010
Cette seule étude apparaît bien modeste en face de la multitude d'études parues ces dernières années qui démontrent l'inverse.
Par exemple le dossier complet par Autier/Boniol en 20017 , "dépistage mammographique, un enjeu en médecine".
L' étude Zielonke a le format d’une méta-analyse, sans en être une et surtout sans en avoir les qualités. Elle utilise des études dites de cohortes et de cas-témoins que la fondation indépendante des chercheurs nordiques Cochrane refuse d'incorporer ; ces études surestiment la valeur de ce qui est recherché et compromettent la qualité des résultats obtenus.
Or l' étude de ZIELONKE a incorporé :
17 études cas témoins (une étude ayant tous les critères de qualité aux yeux des auteurs ne comporte même que 57 cas), 38 études de cohortes, 7 essais cliniques dont les auteurs avouent même que 3 d’entre eux sont considérés à haut risque de biais.
Cette étude est donc de très mauvaise qualité selon les standards internationaux dont celui de la Cochrane (Collaboration indépendante de chercheurs nordiques).
Que le Dr DELALOGE fasse référence à cette étude pour affirmer le bénéfice du dépistage du cancer du sein interroge.
L'ETHIQUE
Un autre argument mis souvent en avant par le Dr DELALOGE est celui de l'éthique, comme nous le voyons dans la deuxième partie de la phrase sus-citée dans l'article du BMJ. "That would not be ethical at all.”
A propos de l'impossibilité d'un bras sans dépistage, le Dr DELALOGE semble oublier que 50% des femmes invitées au dépistage de masse ne s'y rendent pas et cela sans que cette non participation leur fasse "perdre des chances" comme en témoignent nombres de publications scientifiques.
Il n'y a donc aucun problème éthique à proposer un bras sans dépistage.
Par ailleurs, ce n'est pas qu'un bras sans dépistage soit infaisable, c’est que les promoteurs du dépistage dans nos pays occidentaux ne le souhaitent pas.
Un bras sans dépistage est tout à fait réalisable si la volonté existe.
Le risque, pour les promoteurs, est que ce bras sans dépistage pourrait conclure dans l’étude MyPEBS à la supériorité du non-dépistage, ce qui exposerait à conduire à un démantèlement du dispositif de dépistage, éventualité qu'il fallait à tout prix écarter.
Néanmoins cette affirmation de défaut éthique pourrait être acceptable si le dépistage avait montré, sans contestation possible, qu’il permettait de sauver des vies de femmes menacées par le cancer du sein. Dans ce cas, ne pas soumettre les femmes au dépistage serait vraiment une « perte de chance » pour elles comme l'affirme le Dr DELALOGE. Mais de nombreuses études récentes nous disent que ce n'est pas le cas, bien au contraire. Donc, l'étude sans bras dépistage est donc parfaitement éthique et faisable.
L'influence du lobby pro-dépistage.
Le Dr DELALOGE rajoute dans l’interrogation du BMJ sur l’étude MyPEBS contestée par les 4 associations européennes : « Il a été difficile de concevoir une étude visant à cibler le dépistage sur les femmes qui en ont le plus besoin, et à obtenir l'approbation de certains comités d'éthique, qui avaient «très peur» de réduire la fréquence des mammographies chez les femmes à faible risque »
Si ces comités d’éthique en particulier français refusaient le bras sans dépistage, c’est parce que la propagande sur l’utilité du dépistage du cancer du sein par mammographie est très puissante et fait fi constamment des données scientifiques indépendantes sur le sujet.
Chacun connaît la puissance du marketing d’Octobre Rose qui s’affiche chaque année dans tous les médias français, et non contrecarrée par les autorités sanitaires.
Cette affirmation du Dr DELALOGE prouve donc seulement que les comités d'éthique sont sensibles aux campagnes anxiogènes des pro-dépistages, et non pas que cela ne soit pas éthique.
A ce propos, utiliser la peur pour instrumentaliser l’éthique pose question.
Le surdiagnostic, problème majeur de tous les dépistages est minoré.
Le surtraitement ne semble hélas pas préoccupant pour les concepteurs de MyPEBS, il n'est pas même évoqué dans la brochure de consentement donnée aux femmes, même si Mme Delaloge se récrie que la notion de surdiagnostic est bien mentionnée dans plusieurs occurrences de la brochure. Il n'est jamais mis en lien avec le surtraitement qui est la matérialisation concrète pour les femmes de ce risque majeur du dépistage.
Notons encore que le Dr DELALOGE ne le mentionne qu'à son estimation la plus basse, 10%, alors que justement l'éthique, ainsi que la rigueur scientifique imposent de citer aussi les autres évaluations moins optimistes. Il aurait aussi fallu citer celles qui peuvent aller jusqu'à 30% voire 50% de surdiagnostic (https://cancer-rose.fr/2019/09/06/le-depistage-mammographique-un-enjeu-majeur-en-medecine/)..
Un autre point de nos préoccupations éthiques à prendre en compte est celui de l'irradiation annuelle.
Tout d'abord l'utilisation de la tomosynthèse, intégrée dans l'étude MyPEBS, n'est pas encore agrée par l'HAS dans le cadre du dépistage.
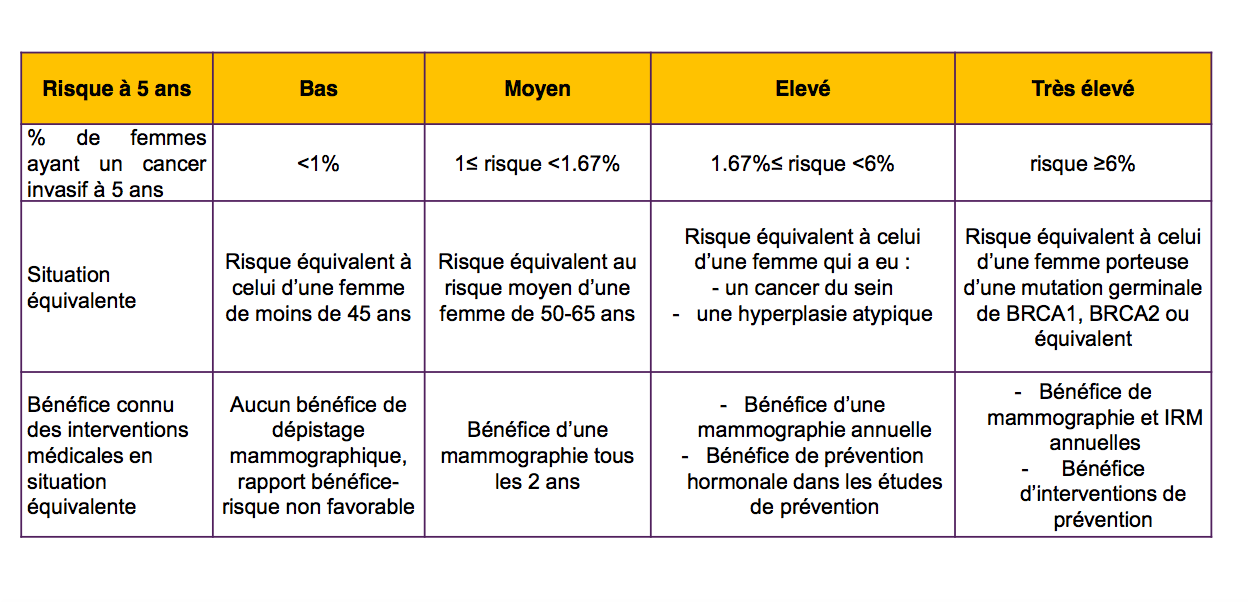
Ensuite, pour les femmes à haut risque et à celles à risque très élevé, c'est à dire à risque équivalent d'une femme porteuse du gène de mutation BCRA, on se garde bien de multiplier les examens ionisants car les radiobiologistes nous alertent depuis longtemps sur ce sur-risque chez les femmes mutées, chez lesquelles déjà le premier examen mammographique est potentiellement inducteur de carcinogénèse (https://www.medecinesciences.org/en/articles/medsci/full_html/2013/05/medsci2013294p397/medsci2013294p397.html
https://www.sfmn.org/drive/CONGRES/JFMN/2016%20GRENOBLE/SCIENTIFIQUE/CommunicationsOrales/N._FORAY_MembreWeb.pdf), mais ce point n'a visiblement pas interpellé la fibre éthique des promoteurs.
LA METHODE CHOISIE
Dans la dépêche apm, Mme Delaloge explique :
"Au cours de l'étude, certaines femmes auront moins de mammographie que le standard actuels. Il est donc indispensable de démontrer que cette stratégie n’est pas délétère".
Nous sommes encore dans la "croyance" que plus l'on réalise de mammographies chez la femme, mieux elle est protégée. Cette "croyance" se heurte à nouveau aux études scientifiques indépendantes.
A la lecture du rationnel, pourtant, rien n'est moins sûr :
(voir : https://cancer-rose.fr/my-pebs/2019/12/01/le-rationnel-de-letude-2/
"À ce jour, les dommages supplémentaires (mammographies faussement positives, possibles surdiagnostics, biopsies rétrospectives inutiles, mammographies faussement négatives) et les bénéfices supplémentaires de l’utilisation de l’information sur les risques polygéniques afin d'adapter les stratégies de dépistage (décès par cancer du sein évités, années de vie sauvées ajustées à la qualité de vie, réduction de la mortalité par cancer du sein) demeurent non testées et inconnues."
Les risques et leur ampleur sont donc parfaitement inconnus, ce qui fait qu'on ne peut proclamer en préambule que l'étude servira à diminuer les risques si on n'en sait rien.
"Chez les personnes à risque élevé, même si les méfaits du dépistage ne diminueront pas et peut même augmenteront en raison d’une fréquence de dépistage plus élevée, ce dépistage a de grandes chances d’être plus efficace, comme le démontrent de nombreuses publications."
Mais les publications mentionnées dans le protocole ne sont pas des études randomisées, seulement des études en modélisation, c'est à dire des hypothèses abstraites !
Les promoteurs justifient donc le choix d'un essai de non-infériorité par la promesse de moins de dommages collatéraux et moins de cancers graves... tout en annonçant plus loin qu'ils ne savent pas où on va, que l'option d'une possible augmentation jusqu'à moins de 25% de cancers graves est bien envisagée (puisque c'est le design de l'étude), et qu'ils veulent étudier ces dommages collatéraux parce qu'ils ne savent pas combien il va y en avoir.
LE PROBLEME DES CANCERS GRAVES EN PLUS
Dans l'article du BMJ, le Dr DELALOGE qualifie de "fou" le fait de penser qu'il y aurait davantage de cancers graves. Or cette hypothèse est envisagée, et est inscrite noir sur blanc dans le protocole lui-même :
Pages 77et 78, point 8.1 du rationnel il est dit : "dans le groupe standard il est attendu 204 cas de cancer de stade 2 ou plus"....puis il est dit plus loin que "la non infériorité sera atteinte (compte tenu des différentes hypothèses faites) s'il y a moins de 298 cancers de stade 2 ou plus dans le groupe dépistage personnalisé." Le protocole accepte donc bien jusqu'à 298 cancers graves en plus, ce qui est un chiffre considérable.
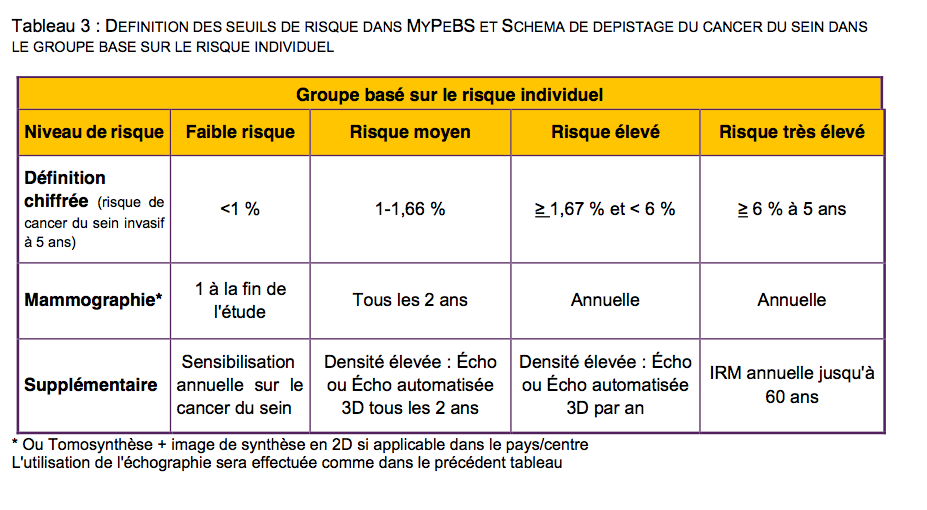
LES NIVEAUX DE RISQUE DANS LE GROUPE DEPISTAGE INDIVIDUEL
Le logiciel d'évaluation du risque individuel.
Comme nous l'avions démontré, le logiciel d'attribution des risques ne dispose d'aucune validation scientifique indépendante, mais d'études faites par des membres pilotant l'étude MyPEBS, et certaines n'ont pas été publiées.
Pour cela veuillez vous reporter à notre analyse en suivant le lien : https://cancer-rose.fr/my-pebs/2019/05/27/le-logiciel-mammorisk/
Cela n'empêche pas le Dr DELALOGE d'affirmer dans la dépêche: "L’évaluation du risque individuel de cancer du sein par des scores de risque cliniques associés à un score de polymorphismes aujourd’hui un bon niveau de validation rétrospectives dans de grandes études internationales."
Nous aimerions avoir communication de ces grandes études internationales dont le Dr DELALOGE fait état car nous n'en avons aucune connaissance.
En effet, les études citées ne sont pas des études d'envergure internationale, comme vous pouvez le voir sur l'article "le logiciel Mammorisk" sus-cité.
De plus, nous avons à disposition des études plutôt défavorables sur l'effective utilité de ces logiciels de prédiction :https://cancer-rose.fr/my-pebs/2019/04/27/une-revue-systematique-et-une-evaluation-qualite-des-modeles-individualises-de-prediction-du-risque-de-cancer-du-sein/
Dans la majorité des pays participant à l'étude MyPeBS, les autorités de santé évitent totalement aux femmes de 40 à 50 ans des mammographies inutiles puisqu'elles considèrent que le dépistage n'a pas lieu d'être. A l'inverse, avec l'étude MyPebs, en ayant choisi une étude de non infériorité, il va devenir possible d'étendre ce dépistage aux femmes de 40 à 50 ans puisque dans un bras il n'y a pas de dépistage actuellement et que dans l'autre bras il y aura dépistage.
Est-il raisonnable, même pour une étude scientifique, de faire subir à des femmes jeunes un dépistage que l'on sait aujourd'hui porteur de risques non négligeables et cela pour un bénéfice hypothétique?
C'est une vrai question éthique que les promoteurs de cette études ne se sont encore une fois visiblement pas posée.
CONCLUSION
Comme il est dit dans la présentation de l'étude, MyPEBS doit servir à établir les prochaines recommandations européennes.
Comme nous venons de le démontrer, les promoteurs de cette étude affirment beaucoup de choses sans en apporter la preuve en particulier dans le cadre méthodologique de cette étude.
Par ailleurs, beaucoup d'inquiétudes dont les femmes participantes devraient être informées, sont soit ignorées soit niées.
Nous comprenons bien qu'en réalité, la véritable finalité de cette étude est d'asseoir le dépistage, l'étendre aux femmes jeunes, et faire en sorte que ce soit l'UE qui recommande le dépistage en Europe sur la base de cette étude.
A ce propos lire aussi : https://cancer-rose.fr/my-pebs/2019/11/01/letude-mypebs-pourra-t-elle-deboucher-sur-de-nouvelles-recommandations-europeennes/