23 février 2020
Quatre collectifs européens, engagés dans la lutte pour l'intégrité en santé, se sont unis pour faire part aux patientes enrôlées dans l'étude ainsi qu'aux médecins sollicités de leurs inquiétudes communes.
Vous trouverez ci-dessous le communiqué de presse ainsi que la lettre, rédigée en langue française, anglaise et italienne.
Communiqué de presse
LETTRE EN FRANçAIS, cliquez :

Une précision concernant notre dénonciation du surdiagnostic : nous avions au préalable une version non définitive de la brochure d'information ; dans l'actuelle le surdiagnostic y est bien mentionné, mais toujours sans faire le lien avec le surtraitement, et à sa fourchette la plus basse (10%), alors que même l'évaluation de l'INCa va jusqu'au taux de 20%.
LETTRE EN ANGLAIS, cliquez :

LETTRE EN ITALIEN, cliquez

RETOUR PRESSE :
Article JIM
https://cancer-rose.fr/my-pebs/wp-content/uploads/2020/10/Capture-décran-2020-03-07-à-16.43.49.png
Article BMJ
ARTICLE BMJ EN FRANçAIS
Article Quotidien du Médecin du 12 mars 2020
_______________________________________________
Prise de position sur le site MyPEBS de la coordinatrice principale, notre lettre aux investigateurs :
Suite à notre lettre ouverte 4 collectifs sur l'étude européenne MyPEBS pour un dépistage individualisé du cancer du sein, Mme le Dr Delaloge y a pris position sur le site dédié à l'étude.
Nous répondons de notre côté, point par point, notamment sur l'étude Zielonke que mentionne Me le Dr Delaloge, publiée par le consortium Eu-Topia, dont l'objectif est "d'améliorer les programmes de dépistage du cancer existants et donc les résultats pour la santé des citoyens européens, ainsi que d'améliorer le rapport coût/efficacité et l'équité à travers l'Europe." (https://eu-topia.org/about-eu-topia/objectives/)
12 mars, par Dr A. Rauss, médecin et biostatisticien, et Dr C.Bour
Après la parution d'une lettre commune co-rédigée avec 4 autres collectifs européens concernant l'étude MyPeBS (publiée dans le journal médical français JIM[1] et reprise dans le BMJ du 03 mars 2020[2]) Mme Delaloge a répondu aux arguments dans un courrier envoyé aux investigateurs le 28/02/2020, et visible sur le site officiel de MyPEBS.
Il nous semble essentiel de vous présenter la réalité des faits pour une décision éclairée.
Après une introduction du contexte nous reprendrons les points les plus critiquables.
Avant toute chose, il nous semble utile de rappeler (comme le fait le Dr Jørgensen dans le BMJ) : la finalité du dépistage ne doit pas être de détecter des cancers mais de réduire la mortalité des femmes. En effet, le nombre de cancers détectés est un critère intermédiaire (en lien avec la mortalité globale bien sûr) MAIS qui ne prend pas en compte tout ce qui va avec le dépistage, c’est-à-dire l'efficacité des traitements, la mortalité lié aux effets indésirables des traitements, les faux positifs avec tout le stress et les investigations qui en découlent, les cancers radio-induits et surtout les surdiagnostics responsables de surtraitements pouvant conduire au décès. Or, l'élément principal intéressant pour les femmes c'est de savoir si le dépistage peut leur garantir de voir leur risque global de décès diminué (il ne suffit pas de ne pas mourir du cancer du sein si c'est pour mourir d'une complication du traitement par exemple), ce qui est difficilement appréciable par le chiffrage uniquement des cas de cancers.
La question de l'éthique de l'étude MyPeBS
Comme nous allons le voir, Mme le Dr Delaloge met en avant la notion d'éthique pour réaliser l'étude MyPeBS comme elle a été conçue. Il s'agit d'un point crucial puisque l'éthique doit guider nos actions. Plusieurs éléments :
- Pour affirmer le caractère éthique du bras dépistage standard, il faudrait que le dépistage ait montré, sans contestation possible, qu’il permet de sauver des vies de femmes menacées par le cancer du sein (ne pas soumettre les femmes au dépistage serait alors une « perte de chance » pour elles); Or, c'est loin d'être le cas.
- Le dépistage du cancer du sein lancé par les grandes campagnes nationales dans les années 90/2000, l'a été du fait du poids sociétal du cancer du sein et devant une théorie qui laissait entendre que si on dépiste les cancers tôt, on devrait voir baisser la mortalité par cancer du sein et baisser les mutilations que cette maladie engendre. Ainsi, faute de mieux, le dépistage dans divers pays a été maintenu, ce qui de loin ne signifie pas une preuve d'efficacité ni qu'il n'est pas contestable et contesté. Cette contestation, de plus en plus pressante, aboutit même, dans certains pays (Australie [3], Québec [4]) à de plans nationaux de réduction de la surmédicalisation tellement le fardeau aussi bien en santé humaine que sur le plan économique apparaît lourd.
- Aujourd'hui, ce n'est pas la publication de 2020 du consortium EU-Topia (l'étude Zielonke dont nous reparlerons) mise en avant par Mme Delaloge qui fait le poids face à la multitude d'études parues ces dernières années qui démontrent l'inverse (tel le dossier Autier/Boniol en 2017 [5] , c’est-à-dire l'absence de preuve d'efficacité face à des effets délétères du dépistage).
- Dans la mesure où déjà 50% des femmes invitées au dépistage de masse ne s'y rendent pas, mettre en place une étude forte pour faire définitivement le point sur l'intérêt éventuel du dépistage aurait assurément permis, moyennant une brochure très complète et explicative sur les tenants et aboutissants d'une non-participation, d'apporter une participation forte de l'ensemble des femmes à cette étude. Ethiquement un tel projet aurait eu du poids aux yeux de toutes les femmes.
- Le surtraitement apparaissait comme une préoccupation forte lors la concertation citoyenne sur le dépistage (page 123 du rapport final): "Il devient urgent et indispensable de promouvoir des études françaises sur les surdiagnostics et les surtraitements...Nous avons besoin de données en rapport avec les modalités et les populations concernées par le dépistage français". Or, éthiquement, seul un bras sans dépistage aurait pu apporter des informations que les Françaises attendent.
- Notons, en rapport avec ce souhait de la consultation citoyenne d'une information honnête, que la minimisation du surdiagnostic et l'omission du surtraitement aussi bien dans le protocole que dans la brochure de consentement donnée aux femmes lèvent un doute sur l'éthique de MyPeBS.
- Comment parler d'éthique quand le surdiagnostic n'est mentionné qu'à sa fourchette la plus basse, 10%, alors que justement l'éthique, mais surtout l'honnêteté et la probité scientifiques imposent de citer aussi les autres évaluations moins optimistes (qui peuvent aller jusqu'à 30% voire 50% de surdiagnostic). [6] [7]
- Reconnaissons que si la concertation mentionnait le souhait de la prise en compte : "entre autres des facteurs génétiques, qui au vu des progrès actuels dans les techniques d’analyse génétique (réduction des coûts et des délais de résultats), devraient être potentiellement disponibles pour le plus grand nombre" elle ajoutait " à la condition que des évaluations des préconisations proposées à ces femmes soient réalisées avec rigueur" , ce qui éthiquement n'est pas respecté dans MyPeBS puisque le niveau de risque retenu n'est pas sur un modèle de risque validé selon les règles [8].
- La recherche de facteurs génétiques soulève des questions éthiques, que ces facteurs soient modifiables ou non : l’annonce de la présence d’un facteur de risque supplémentaire augmentera-t-elle les chances de lutter contre ce facteur, ou induira-t-elle un stress inutile, voire délétère ? Cette dimension n'est pas abordée par les concepteurs de MyPeBS.
- Les femmes intégrées dans l'étude MyPEBS vont bien donner leur consentement écrit pour le prélèvement et le stockage du matériel génétique. Malgré tout, éthiquement est-on certain que la compréhension des conséquences de tels tests génétiques est assurée ? Toujours éthiquement, Les concepteurs de l'étude se sont-ils préoccupés de vérifier l'acceptation par ces femmes d'une possible annonce de la présence d'un facteur génétique les plaçant dans un groupe à haut risque? Surtout que les femmes le comprendront d'ailleurs aisément spontanément, puisque les femmes à haut risque se voient attribuer un suivi médical annuel, avec un rythme de mammographies plus intense que celles à bas risque... Cette préoccupation était également évoquée elle-aussi par la concertation citoyenne. [9]
- L'irradiation annuelle et l'utilisation de la tomosynthèse dans les centres qui en disposent pour les femmes dans les groupes à haut risque, et pour celles à risque très élevé c'est à dire à risque équivalent d'une femme porteuse de mutation BRCA sont-elles éthiques ? La question mérite d'être posée puisque, normalement, chez ces dernières, on se garde justement bien de réaliser des examens avec radiations ionisantes de façon répétée. Les radiobiologistes nous alertent depuis longtemps sur ce sur-risque chez les femmes mutées, chez lesquelles le premier examen mammographique est potentiellement inducteur de carcinogénèse. [10] [11]
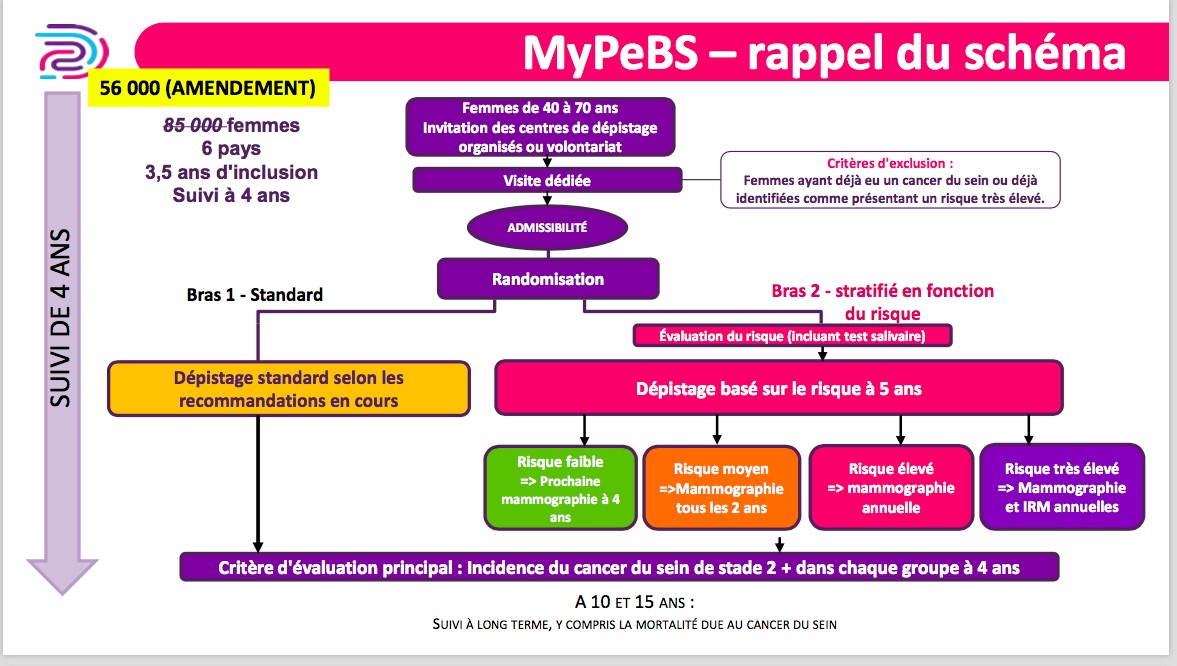
L'éthique de la baisse attendue des cancers graves dans MyPEBS?
Docteur Delaloge a souligné: " Notre hypothèse forte, compte tenu de la stratégie de dépistage proposée, est que nous serons dans la zone de supériorité́ (verte), avec une diminution de l’incidence des cancers de stade 2 et plus. " Car sinon, dit-elle encore dans la lettre du BMJ "ce serait totalement fou" (nous reviendrons sur cette notion d'hypothèse forte).
Malgré tout, les auteurs avouent eux-mêmes, dans le rationnel de l'étude (page 47, point 1.1.25) ne pas savoir du tout à quoi ils s'attendent...et même s'attendent à davantage d'effets adverses: "À ce jour, les dommages supplémentaires (mammographies faussement positives, possibles surdiagnostics, biopsies rétrospectives inutiles, mammographies faussement négatives) et les bénéfices supplémentaires de l’utilisation de l’information sur les risques polygéniques afin d'adapter les stratégies de dépistage (décès par cancer du sein évités, années de vie sauvées ajustées à la qualité de vie, réduction de la mortalité par cancer du sein) demeurent non testées et inconnues."
Les risques et leur ampleur sont donc parfaitement inconnus. On ne peut, éthiquement, proclamer en préambule que l'étude servira à diminuer les risques si on n'en sait rien.
Ethiquement plus grave, pour les femmes à haut risque dans le bras dépistage individuel, ils ne seront pas diminués, on dit bien à ces femmes qu'elles ont un espoir de voir diminuer leur risque de cancer grave, cela au prix de davantage de surdiagnotic et biopsies. Point 1.1.10, page 35 du protocole : "Chez les personnes à risque élevé, même si les méfaits du dépistage ne diminueront pas et pourraient même augmenter en raison d’une fréquence de dépistage plus élevée, ce dépistage a de grandes chances d’être plus efficace, comme le démontrent de nombreuses publications.". On signalera juste que les publications mentionnées dans le protocole ne sont pas des études randomisées, mais seulement des études en modélisation !
En conclusion de cette première partie, mettre en avant le caractère éthique de l'étude MyPeBS pose sincèrement question.
Voyons maintenant le détail des points critique du courrier :
-
Pas de bras « sans dépistage »
Docteur Delaloge dit: "MyPeBS est une étude de « comparative effectiveness » financée par la Commission Européenne dans une dynamique qui vise à challenger et améliorer les pratiques de santé publique en Europe. MyPeBS compare donc une nouvelle stratégie de dépistage individualisé, au standard actuel."
Le standard (ce qui se fait quotidiennement) n'est pas forcément ce qui devrait être fait, il peut exister un temps non négligeable entre une approche définie à un moment donné (le "standard") et la nouvelle approche (le nouveau standard) qui intègre les dernières données de la science.
Docteur Delaloge dit: "Le dépistage du cancer du sein par mammographie est aujourd’hui le standard reconnu par l’immense majorité des autorités de santé, sociétés savantes, et organismes de santé publique des pays occidentaux et d’un grand nombre de pays émergents."
Affirmer cela, c'est nier qu'il existe de très nombreuses études qui infirment l’utilité du dépistage, et c’est nier l’existence dans la majorité des pays d’une contestation du dépistage du cancer du sein par mammographie, contestation qui est loin d’être minoritaire.
D’ailleurs, si la France était si convaincue de l’intérêt de ce dépistage, pourquoi s'est-il tenu en 2015/2016 une concertation citoyenne sur le sujet dont les deux scénarios demandaient l’arrêt de ce dépistage organisé ?
Docteur Delaloge dit: "Les dernières publications Européennes sont claires sur les bénéfices du dépistage mammographique (Zielonke N, Gini A, Jansen EEL, et al. Evidence for reducing cancer-specific mortality due to screening for breast cancer in Europe: A systematic review. Eur J Cancer. 2020;127:191–206. doi:10.1016/j.ejca.2019.12.010)".
Une seule étude est citée et cette étude ne répond pas aux standards de qualité que l’on attend d’une étude. Cette étude a le format d’une méta-analyse, sans être une méta-analyse et sans en avoir les qualités, et ayant plutôt tous les critères d’une étude de très mauvaise qualité.
Ainsi la fondation Cochrane refuse l’incorporation d’études cas témoins ainsi que les études de cohorte dans ses méta-analyses car ces études surestiment la valeur de ce qui est recherché. Incorporer ce type d’études fausse complètement la qualité des résultats obtenus.
Or cette étude de ZIELONKE a incorporé :
17 études cas témoins (une étude ayant tous les critères de qualité aux yeux des auteurs ne comporte même que 57 cas)
38 études de cohortes
7 essais cliniques dont les auteurs avouent même que 3 d’entre eux sont considérés à haut risque de biais.
Que madame le Dr DELALOGE puisse s'appuyer uniquement sur cette étude pour affirmer le bénéfice du dépistage du cancer du sein par mammographie est difficilement compréhensible en 2020.
Docteur Delaloge dit: "Un bras sans dépistage serait totalement hors standard et non éthique : non seulement ce dépistage sauve des vies (cft Zielonke et al pour des données actualisées), mais par ailleurs un groupe sans dépistage aujourd’hui dans des pays occidentaux n’est pas faisable, car il signifierait dépistage individuel basé sur le niveau socio-économique."
- "Un bras sans dépistage hors standard est non éthique":
Nous avons déjà parlé de cette problématique complètement fausse surtout à partir des seules données qui seraient actualisées et qui se trouveraient dans l'étude de Zielonke (dont nous venons de voir la très mauvaise qualité).
Une étude sans bras dépistage était parfaitement éthique
- " un groupe sans dépistage aujourd’hui dans des pays occidentaux n’est pas faisable, car il signifierait dépistage individuel basé sur le niveau socio-économique"
Il est difficile de suivre le raisonnement de Docteur Delaloge sur ce point. En effet, elle semble dire que le dépistage [qui ne démontre plus son utilité] se ferait suivant le niveau socio-économique; or, si le dépistage ne sert à rien, il ne sert à rien quel que soit le niveau socio-économique. Dans ces conditions, quelle que soit la pratique actuelle du dépistage, comme quel que soit le niveau socio-économique, le dépistage ne sert à rien, et il est parfaitement éthique de réaliser une étude avec un bras sans dépistage.
Il est clair qu'une stratégie d'étude avec un bras sans dépistage était tout à fait réalisable si la volonté existait de la concevoir ainsi, compte tenu des données qui existent actuellement.
Le risque, pour les promoteurs de MypEBS, était qu'une telle étude aurait pu conclure à la supériorité du non-dépistage, ce qui exposait à conduire au démantèlement du dispositif de dépistage, éventualité qu'il fallait écarter d'emblée.
-
La méthodologie choisie de non-infériorité
Docteur Delaloge dit: "Il est plus lourd et plus difficile de conduire une étude de non-infériorité."
Cette affirmation est fausse, c'est tout le contraire : dans une situation d'incertitude sur une supériorité d'un effet, il est préférable d'envisager une étude de non infériorité. Ainsi, si l'étude ne permet pas de conclure à la supériorité, elle permettra, au moins, de conclure à la non infériorité. Ces dernières années, l’industrie pharmaceutique, a bien compris l'intérêt de ce type d'étude. Elle a introduit dans nombre de ses essais cliniques le choix d'une étude de non-infériorité pour ses nouveaux médicaments. En effet, quand l'industrie a des doutes sur une éventuelle supériorité d'un médicament elle envisage une étude de non infériorité avec la possibilité de faire de la supériorité secondairement (comme dans MyPebs).
Partir directement sur une étude de supériorité est souvent considéré comme bien trop risqué et pourrait aboutir à aucune conclusion.
Or, ce qui est particulièrement recherché par les auteurs de MyPeBS face au déclin du dépistage : Faire une étude qui permette à tout coup de conclure. Si le dépistage sur les risques individuels n'est pas supérieur au dépistage standard, AU MOINS, il faut pouvoir conclure que : quelle que soit l'approche de dépistage retenue aucune des deux ne soit inférieure l'une à l'autre.
L’étude de non-infériorité transformable en supériorité serait donc la bonne stratégie à adopter.
MALGRE TOUT, pour que cette approche soit au minimum acceptable dans MyPeBS et que la conclusion à venir de l'étude est un sens, il faudrait que le "traitement standard" (ici le dépistage standard) soit utile et bénéfique ce qui n’est justement pas démontré.
En choisissant une étude de non infériorité les auteurs ne le font pas pour faire avancer la "science" mais pour avoir l'assurance que quelle que soit la conclusion, le dépistage sortira renforcé de l'étude. On retrouve ici ce point essentiel qui NECESSITAIT que l'étude ne soit pas avec un bras sans dépistage pour assurer la conclusion voulue des auteurs.
Docteur Delaloge dit: "Nous avons cependant choisi ce design car MyPeBS est en partie une étude de « désescalade » de prise en charge. Certaines femmes auront moins de mammographie que le standard actuel. Il est donc indispensable de démontrer que cette stratégie n’est pas délétère (« primum non nocere »). Pour cela nous avons choisi une non infériorité en première intention. Mais cette stratégie de dépistage ne pourrait devenir un standard que si une supériorité était démontrée, la supériorité est donc le premier objectif secondaire".
Si certaines femmes auront moins de mammographies, les auteurs de MyPeBS disent eux-mêmes dans le protocole, qu'au final il y aura une augmentation des mammographies. Vouloir présenter l'étude comme une étude de désescalade qui justifierait le recours à une étude de non infériorité est peu cohérent.
Docteur Delaloge dit: "Les critiques formulées sur une potentielle augmentation de 25% des taux de cancers avancés chez les femmes participant à l’étude sont totalement erronées : le plan statistique a fixé la barre supérieure de l’interv alle de co nfiance pour juger de la non-infériorité à 1.25 (25% d’augmentation de l’incidence de cancers de stade 2 et plus). Il s’agit de la barre supérieure d’un intervalle de confiance !!!
Ce n'est pas ce qui est observé qui compte puisque nous ne travaillons que sur des échantillons. La vraie valeur de l'augmentation est inconnue. On travaille donc toujours avec des intervalles de confiance qui ont 95 chances sur 100 de contenir la vraie valeur. Trouver un Risque Relatif de 1,03 avec un intervalle de confiance de [0,85 – 1,2475] veut simplement dire que la vraie valeur de l'augmentation à 95 chances sur 100 de se trouver dans cet intervalle (cela peut être une diminution de 15% pour la borne inférieure de 0,85 comme cela peut être une augmentation de 24,75% pour la borne de 1,2475. Dire que l'on retient une borne supérieure de non infériorité à 1,25 signifie juste que l'on accepte l'idée que la vraie valeur puisse au maximum être la borne supérieure de l'intervalle de confiance. Ainsi, en retenant une borne à 1,25 les auteurs de MyPeBS acceptent bien l'idée que la vraie valeur de l'augmentation des cancers avec le dépistage personnalisé soit de 25%.
Docteur Delaloge dit: "c’est à dire que même si quelques cas en plus étaient observés, cette limite sera atteinte (rouge). Le schéma ci-dessous sera beaucoup plus explicite pour bien comprendre ce choix !"
Cette présentation est fausse. En effet, dans le protocole de l'étude (P77et 78 point 8.1) il est dit 2 choses: dans le groupe standard il est attendu 204 cas de cancer de stade 2 ou plus (42 500 femmes dans le groupe pour une incidence de 120/100 000 par an: 204=120*4*42500/100 000) et il est dit plus loin que la non infériorité sera atteinte (compte tenu des différentes hypothèses faites) s'il y a moins de 298 cancers de stade 2 ou plus dans le groupe dépistage personnalisé. On est loin des quelques cas en plus (6 cas), chiffre basé sur un calcul basique d'un intervalle de confiance où la limite supérieur de l'intervalle de confiance du risque serait 1,25.
Docteur Delaloge dit: "Notre hypothèse forte, compte tenu de la stratégie de dépistage proposée, est que nous serons dans la zone de supériorité (verte), avec une diminution de l’incidence des cancers de stade 2 et plus".
Si l'hypothèse était vraiment forte, avec une idée d'une diminution de l'incidence des cancers de stade 2 ou plus, alors rien ne justifie plus le choix d'une étude de non infériorité et non d'une étude de supériorité. En fait nous l'avons bien expliqué plus haut, l'hypothèse n'est pas si forte et les auteurs ont absolument besoin de s'assurer qu'une conclusion de deux approches de dépistage non inférieures l'une à l'autre soit la conclusion première de l'étude.
-
Niveaux de risque
Docteur Delaloge dit: "La question de base de MyPeBS est d’évaluer si un dépistage basé sur le risque individuel de cancer du sein est aussi ou plus efficace qu’un dépistage standard où seul l’âge est pris en compte pour faire ou non des mammographies".
Il faudrait savoir: soit l'hypothèse est forte d'une plus grande efficacité du dépistage basé sur le risque individuel ou pas. Annoncer que la question de base est de savoir si le dépistage est aussi efficace que le dépistage standard lève un doute majeur sur "l'hypothèse forte" présentée plus haut.
Docteur Delaloge dit: "25% des cancers du sein surviennent avant 50 ans (beaucoup plus dans d’autres pays moins favorisés) avec des taux de cancers avancés plus élevés que chez les femmes plus âgées."
Cette phrase est incompréhensible. Soit il s'agit d'un scoop avec la révélation d'un nouveau facteur de risque de cancer du sein: le niveau économique d'un pays, soit il s'agit d'un excès d'enthousiasme pour essayer de nous convaincre qu'il faut étendre le dépistage au maximum.
Docteur Delaloge dit: "Aujourd’hui, entre 40 et 50 ans, la réalisation ou non d’une mammographie de dépistage dépend du pays, de la région, parfois du médecin, et beaucoup du niveau socio-économique. Notre étude a donc un intérêt particulier chez les femmes les plus jeunes !"
Il est particulièrement curieux de présenter le dépistage de cette façon puisque dans 4 des 5 pays qui participent à l'étude, il n'y pas de dépistage avant 50 ans et dans le 5ème pays, seules certaines régions font ce dépistage.
Docteur Delaloge dit: "La plupart d’entre elles (60%) seront classées à risque faible, ce qui permettra justement de leur éviter des mammographies inutiles actuellement réalisées ! Les femmes qui ont réellement besoin de mammographies devraient être identifiées au contraire, alors qu’un grand nombre d’entre elles ne le sont pas."
La présentation de Dr Delaloge nous semble très osée puisqu'aujourd'hui, dans la majorité des pays participants à l'étude MyPeBS, les autorités de santé évitent totalement aux femmes de 40 à 50 ans des mammographies inutiles puisqu'elles considèrent que le dépistage n'a pas lieu d'être!
A l'inverse, avec l'étude MyPebs, en ayant choisi une étude de non infériorité, il va devenir possible d'étendre ce dépistage aux femmes de 40 à 50 ans puisque dans un bras il n'y a pas de dépistage actuellement et que dans l'autre bras il y aura dépistage. La conclusion de l'étude sera alors: chez les femmes de 40 à 50 ans, les deux approches sont comparables, pas de dépistage ou dépistage basé sur le risque individuel. On pourra donc instaurer du dépistage sans problème chez les quadragénaires.
Docteur Delaloge dit: "L’évaluation du risque individuel de cancer du sein par des scores de risque cliniques associés à un score de polymorphismes a aujourd’hui un bon niveau de validation rétrospectives dans de grandes études internationales dont de nombreuses récentes."
Il est étonnant pour ne pas dire choquant de voir le Dr Delaloge laisser entendre que l'évaluation du risque individuel est aujourd'hui validée alors que les auteurs de l'étude disent, eux-mêmes, dans leur protocole que le niveau de risque individuel en 4 catégories a été établi par le steering commitee de l'étude et non sur la base d'une étude de validation.
La validation du logiciel, elle-même, ne repose sur aucune étude indépendante, ce que nous démontrons dans l'analyse accessible sur notre site MyPEBS.[12]
-
Enjeux économiques
Docteur Delaloge dit: "MyPeBS ne peut pas tout faire, et financer cette étude est un choix de la Commission Européenne, où ce projet a été un des 6 sélectionnés parmi 200 soumis. La Commission Européenne demande que ce projet, après analyse de tous les résultats et de toutes les composantes, fournisse à l’UE des recommandations pour le futur du dépistage du cancer du sein en Europe".
En disant cela, Dr Delaloge nous révèle la véritable finalité de cette étude: Faire que ce soit l'UE qui recommande le dépistage en Europe sur la base de cette étude.
Références
[1] https://www.jim.fr/e-docs/interrogations_sur_l_etude_mypebs_pour_un_depistage_personnalise_du_cancer_du_sein_181909/document_edito.phtml
[2] https://www.jim.fr/e-docs/interrogations_sur_l_etude_mypebs_pour_un_depistage_ personnalise_ du_cancer_du_sein_181909/ document_edito.phtml
[3] https://cancer-rose.fr/2018/10/15/un-plan-daction-national-contre-le-surdiagnostic-en-australie/
[4] https://www.preventingoverdiagnosis.net/2014presentations/surdiagnotsic-plan-action-fr(Abs57).pdf
[5] https://www.ejcancer.com/article/S0959-8049(17)31385-0/abstract
[6] https://www.bmj.com/content/359/bmj.j5224
[7] https://annals.org/aim/article-abstract/2596394/breast-cancer-screening-denmark-cohort-study-tumor-size-overdiagnosis
[8] https://cancer-rose.fr/my-pebs/2019/05/27/le-logiciel-mammorisk/
[9] page 121 du rapport de la concertation : "Progrès scientifiques: une meilleure connaissance des facteurs de risque individuels de survenue d’un cancer du sein devrait avoir pour objectif d’adapter les modalités du dépistage { chaque femme (rythme de surveillance, modalités d’imagerie ...en fonction des risques). Il s’agit entre autres des facteurs génétiques, qui au vu des progrès actuels dans les techniques d’analyse génétique (réduction des coûts et des délais de résultats), devraient être potentiellement disponibles pour le plus grand nombre, à la condition que des évaluations des préconisations proposées à ces femmes soient réalisées avec rigueur. Notons aussi que la recherche de facteurs génétiques soulève des questions éthiques, que ces facteurs soient modifiables ou non: l’annonce de la présence d’un facteur de risque supplémentaire augmentera-t-elle les chances de lutter contre ce facteur, ou induira-t-elle un stress inutile, voire délétère ?"
[10] https://www.sfmn.org/drive/CONGRES/JFMN/2016%20GRENOBLE/SCIENTIFIQUE/CommunicationsOrales/N._FORAY_MembreWeb.pdf
[11] https://studylibfr.com/doc/2144805/radiosensibilite-individuelle---une-notion-ancienne-et-so...
[12] https://cancer-rose.fr/my-pebs/2019/05/27/le-logiciel-mammorisk/